Tiêm phòng cúm cho mẹ bầu: Lời khuyên từ chuyên gia (Phần 2)

Chuyên gia viết bài: PGS.TS.BS. Cao Hữu Nghĩa
Chủ nhiệm Bộ môn Khoa học Y sinh, Viện Pasteur TP.HCM
Ngày cập nhật: 28/08/2025
Mục lục
- Khi nào tiêm vaccine thì phù hợp?
- Thời điểm nào trong năm dễ mắc cúm mùa
- Tình hình lưu hành cúm tại Việt Nam
- Vaccine cúm tứ giá là gì? Sự phát triển của vaccine từ đơn giá đến tứ giá?
- Mẹ bầu có thể dùng loại vaccine cúm tứ giá nào?
- Vaccine cúm tứ giá, bất hoạt có những loại thường gặp nào?
- Vaccine cúm tứ giá tiểu đơn vị có gì khác biệt?
- Những lưu ý sau tiêm vaccine cúm
Khi nào tiêm vaccine thì phù hợp?
Phụ nữ mang thai có thể tiêm phòng cúm trong bất kỳ giai đoạn nào của thai kỳ. Tuy nhiên, ưu tiên bảo vệ phụ nữ trong 3 tháng giữa và 3 tháng cuối của thai kỳ vì đây là thời điểm dễ xảy ra các biến chứng nghiêm trọng do cúm. Sau khi chủng ngừa, thường mất đến 2 tuần để phát huy tác dụng bảo vệ.
Phụ nữ đã tiêm vaccine trước khi mang thai cần được tiêm lại trong thời kỳ mang thai để bảo vệ thai nhi.
Điều quan trọng không kém là những người khác trong gia đình cũng cần được chủng ngừa cúm. Các thành viên trong gia đình cần tiêm phòng cúm 2 tuần trước khi mùa cúm bắt đầu.

Thời điểm nào trong năm dễ mắc cúm mùa
Theo tổ chức WHO, tại các vùng ôn đới, dịch cúm mùa thường xảy ra vào mùa lạnh. Và tại các vùng nhiệt đới, bệnh thường xảy ra quanh năm với các đợt bùng phát bất thường.
Tại Việt Nam bệnh cúm xuất hiện quanh năm và thường có 1-2 đỉnh dịch/năm, gia tăng vào tháng 3 – 4 và tháng 9-10 hằng năm.
Tình hình lưu hành cúm tại Việt Nam
Mỗi năm, Hệ thống Giám sát và Ứng phó với Cúm của WHO sẽ đánh giá sự biến đổi của virus cúm, và đưa ra khuyến cáo về thành phần vaccine cho mùa cúm tiếp theo trong mỗi bán cầu
Đối với các quốc gia ở Bắc bán cầu: vaccine được sử dụng có “công thức Bán cầu bắc“, phản ánh các chủng virus dự kiến sẽ lưu hành trong mùa đông Bắc bán cầu.
Tương tự ở Nam bán cầu: Vaccine thuộc “công thức bán cầu Nam” sẽ được sử dụng, phản ánh các chủng virus dự kiến lưu hành trong mùa đông ở Nam bán cầu.
Việt Nam tuy thuộc Bắc Bán Cầu, nhưng chủng cúm lưu hành tại nước ta có sự kết hợp giữa các chủng virus từ cả khu vực Bắc bán cầu và Nam bán cầu.
Vaccine cúm tứ giá là gì? Sự phát triển của vaccine từ đơn giá đến tứ giá?
Vaccine cúm tứ giá là một loại vaccine tổng hợp, được sản xuất để bảo vệ cơ thể chống lại 4 chủng virus cúm khác nhau.
Sự phát triển từ vaccine đơn giá đến tứ giá:
- Virus cúm A xuất hiện, vaccine cúm đơn giá đầu tiên ra đời
- Virus cúm B xuất hiện, vaccine nhị giá được phát triển để bảo vệ người dân khỏi cả 2 chủng cúm A và B
- Trước 2 chủng cúm A (H1N1 và H3N2) và 1 chủng cúm B, vaccine tam giá được phát triển
- Sự phân hóa của virus cúm B thành 2 chủng riêng biệt (Victoria và Yamagata) đã dẫn đến sự phát triển của vaccine cúm tứ giá

Mẹ bầu có thể dùng loại vaccine cúm tứ giá nào?
Các loại vaccine cúm tiêm cho phụ nữ mang thai đều là vaccine cúm bất hoạt – chứa các virus cúm đã chết nên không có khả năng gây bệnh cũng như không ảnh hưởng đến sức khỏe của mẹ bầu và thai nhi.
Các loại vaccine cúm tứ giá, bất hoạt được cấp phép tại Việt Nam có thể phù hợp cho mẹ bầu.
Vaccine cúm tứ giá, bất hoạt có những loại thường gặp nào?
Theo quá trình phát triển của vaccine, thành phần trong công thức vaccine cúm cũng ngày càng hoàn hiện hơn. Một số loại vaccine cúm tứ giá, bất hoạt có thể kể đến như:
Vaccine toàn phần – virus cúm nguyên vẹn được bất hoạt
Vaccine phân mảnh – virus được bất hoạt, phân cắt, chứa hàm lượng cao các thành phần cần thiết để tạo ra miễn dịch
Vaccine tiểu đơn vị – virus được bất hoạt, phân cắt và tinh chế để chọn lọc các thành phần cần thiết
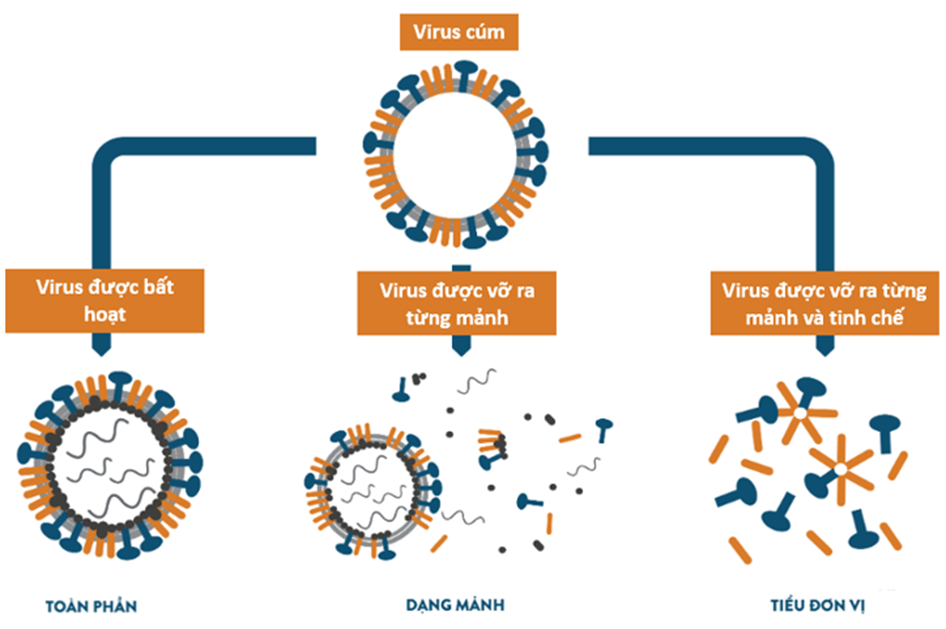
Vaccine cúm tứ giá tiểu đơn vị có gì khác biệt?
Vaccine cúm tứ giá tiểu đơn vị có khả năng tạo ra miễn dịch để bảo vệ cơ thể khỏi virus tương đương so với vaccine phân mảnh, và ít gây phản ứng tại chỗ và phản ứng toàn thân hơn.
Vì chỉ chứa các thành phần cần thiết để tạo miễn dịch, và không chứa các thành phần khác của virus, khả năng gây ra phản ứng có hại của vaccine tiểu đơn vị là rất thấp.
Nhờ đó, vaccine cúm tứ giá tiểu đơn vị phù hợp cho nhiều đối tượng như trẻ em, người lớn, người cao tuổi và phụ nữ mang thai.

Chủ nhiệm Bộ môn khoa học Y sinh, viện Pasteur TP.HCM
Những lưu ý sau tiêm vaccine cúm
Sau khi tiêm vaccine cần lưu ý tác dụng phụ chủ yếu là đau ở vị trí tiêm. Ngoài ra, có thể xuất hiện các triệu chứng toàn thân như đau cơ, nhức đầu, sốt nhẹ, buồn nôn,… Thường thì những triệu chứng này nhẹ và tự hết hoàn toàn trong từ 1 – 2 ngày. Nếu các triệu chứng kéo dài hơn 2 ngày thì các mẹ cần liên hệ bác sĩ để được tư vấn.
Tương tự với các vaccine khác, mẹ bầu sẽ được theo dõi các tác dụng phụ sau khi tiêm vaccine cúm từ 15-30 phút.
Xem thêm:
- Tiêm phòng cúm cho mẹ bầu: Lời khuyên từ chuyên gia (Phần 1)
- Tiêm phòng cúm cho mẹ bầu: Lời khuyên từ chuyên gia (Phần 3)
- Những điều cần biết về tiêm phòng cúm cho mẹ và bé












